
15399414884
前世今生——环状RNA的发生及发展
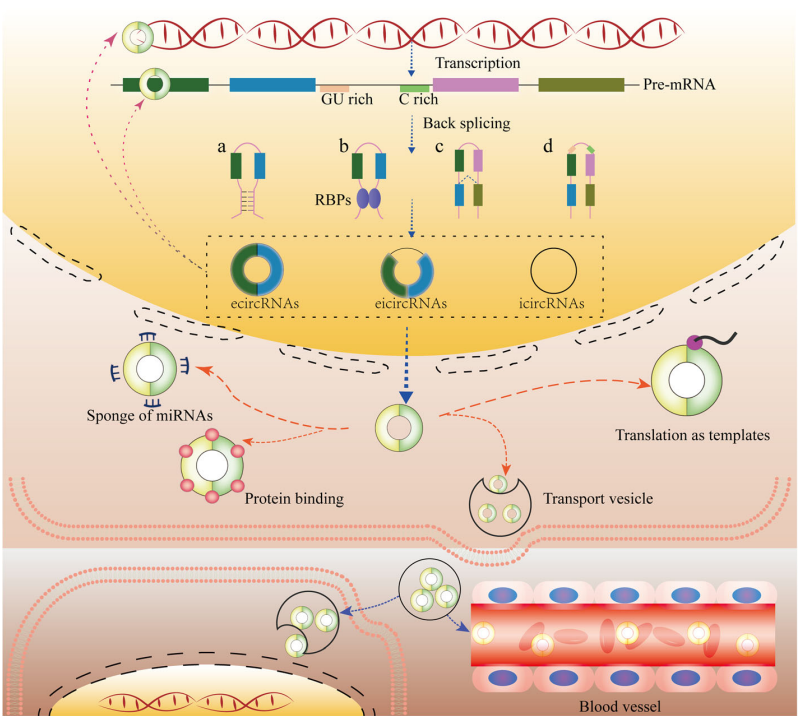
环状RNA(circRNA)是真核生物中新近发现的一类非编码RNA,通常由外显子组成,具有由前体mRNA反向剪接形成的环状构型,没有5′端帽子结构和3′端多聚腺苷酸尾巴。因其特殊的环状结构,circRNA对核酸外切酶具有较强的抗性,导致其半衰期比线性RNA长。CircRNA自1976年首次提出以来就被定义为剪接过程中产生的“垃圾”,不具有任何功能。随着二代测序技术的快速发展,人们鉴定了数千种不同基因产生的circRNA,它们已被证实是参与多种生理和病理过程的关键调控因子。例如,CircCCDC9通过海绵miR-6792-3p靶向CAV1蛋白抑制胃癌的增殖。Circular RNA MTCL1特异性结合C1QBP蛋白,通过抑制其泛素化降解并介导β-catenin蛋白活化以促进晚期喉鳞状细胞癌进展。
异军突起——环状RNA正在成为RNA疗法的下一代重要技术
众所周知,新冠肺炎在过去三年间加速了地理传播,给全球人民带来了难以估量的损失。如今,新冠肺炎依然是对人类健康的潜在威胁。在这场全球大流行病中,mRNA疫苗闪亮登场并创下了历史上疫苗开发的最快纪录。因此,为了表彰mRNA疫苗在抗击新冠大流行中的重要作用,诺贝尔官方将2023年生理学或医学奖授予了两位mRNA技术奠基人卡塔琳·卡里科(Katalin Karikó)博士和德鲁·魏斯曼(Drew Weissman)博士。
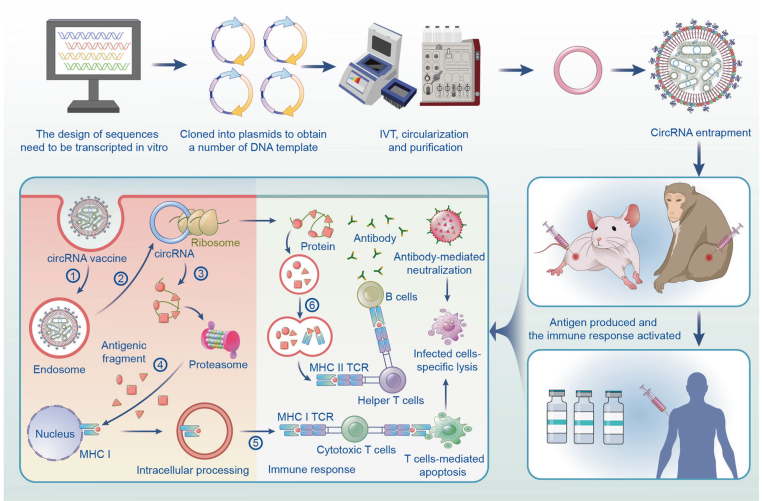
线性mRNA疫苗虽然研发周期短且易于实现量产,但人们也知道这一技术存在若干缺点。首现,RNA通常是线性形式,寿命较短,几个小时内,细胞中的核酸酶就会降解掉RNA。虽然RNA转瞬即逝的性质对疫苗来说并不是什么大问题,但是对于大多数治疗应用来说,拥有可以停留更长时间的RNA可能具有更长的疗效。此外,线性mRNA疫苗存在低效性以及先天免疫原性限制等问题。最后,mRNA疫苗从装瓶到接种前一刻,都需要及其严苛的运输及储存条件。幸运的是,circRNA体外合成的突破使得circRNA将成为下一代RNA疗法的基石。与疫苗中使用的标准线性mRNA相比,circRNA具有多种优势。CircRNA表现出高稳定性和RNase抗性,使得其在室温或反复冻融条件下不会降解。未修饰的circRNA具有较小的副作用,安全性能高。CircRNA可以延长抗原递呈时间并保持持久的免疫反应,即使在低剂量的水平,也可以增加其治疗潜力。这些特点将使环状RNA正在成为制药行业首选的RNA平台,并可能推动罕见病治疗、新一代抗癌药物等产品的出现。
未来可期——环状RNA疫苗在疾病中的潜在应用
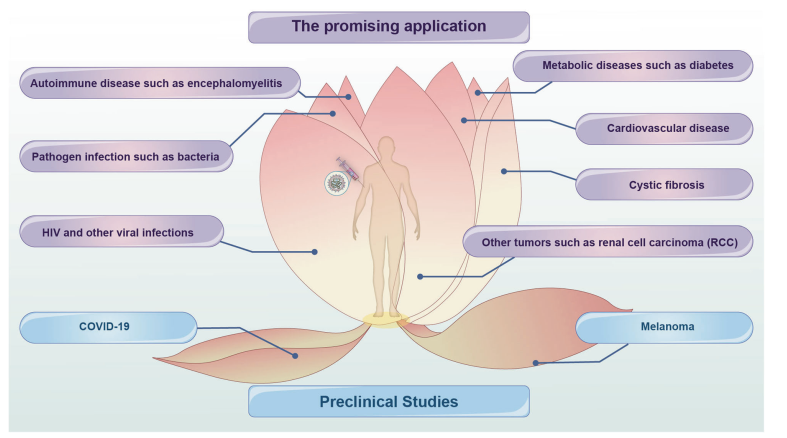
CircRNA作为下一代RNA疗法的核心,有望治疗各种难治性疾病,包括病毒性传染病、肿瘤、病原菌感染、自身免疫性疾病、代谢性疾病等。目前circRNA已成功应用于几种Sars-CoV-2疫苗,这些疫苗可以产生更高比例的中和抗体。例如,circRNA疫苗(VFLIP-X)使用LNP递送系统,通过肌肉注射5μg circRNA进行免疫,在小鼠体内能够针对Sars-CoV2各种突变体产生强大中和抗体反应。此外,Hongjian Li等人报道了一项基于circRNA疫苗治疗黑色素瘤的研究,他们发现这种circRNA疫苗在小鼠体内能够显著抑制肿瘤转移并表现出令人欣喜的免疫疗效。
CircRNA虽然弥补了mRNA的诸多缺点,但是circRNA疫苗的开发仍处于初级阶段。随着相关研究的不断推进,我们相信基于circRNA的新一代RNA疗法将成功应用于各种疾病的治疗和预防。